DH Anasayfa
İndirim Kodu
Ara
Popüler
Foruma Git
Hakkımızda
Destek
Mobil Sürüm
Standart Site Görünümü
Bu konudaki kullanıcılar: 1 misafir, 1 mobil kullanıcı
24
Cevap 10206
Tıklama 0
Öne Çıkarma
Cevap 10206
Tıklama 0
Öne Çıkarma
-
Kimya Entalpi Sorularım
Cevap Yaz
Konuya Özel
| bunlar basit de dostum bu kadarını kim çözecek 2-3 tane soru yollasan neyse |
Bu mesaja 1 cevap geldi. Cevapları Gizle
hepsinin çözümünü istemedim aralarından farklı tiplerde birkaç tane tane yapsanız yeter benim için örnek olması bakımından , dediğim gibi konuyu bilmiyorum  |
Bu mesaja 1 cevap geldi. Cevapları Gizle
|
farklı soru tiplerinden 1-2 tane çözseniz işimi görür yardım lütfen |
Bu mesaja 1 cevap geldi. Cevapları Gizle
fotoğraf çekmem mümkün değil yazıcıdan tarattım resmin üstüne tıklayınca orjinal boyutuna geliyor okunmama gibi bir problem yok , mobil misiniz? |
Bu mesaja 1 cevap geldi. Cevapları Gizle
pardon ya zoom yapılıyomus. biraz bakıcam sorulara. sen ılk sayfayla uğraş ben ikinci sayfayla |
Bu mesaja 1 cevap geldi. Cevapları Gizle
tamam çok teşekkür ederim  |
Bu mesaja 2 cevap geldi. Cevapları Gizle
| 9-10 u çözdüm devam ediyorum |
|
Sisteme iş yapılması veya çıkmasında U=Q+W formülünü kullanıcaksın.Q verilen ısı oluyor giriyorsa (+) alıcan,çıkıyorsa eksi.W ise iş demek,yine aynı şekilde sistem ortama yapıyorsa (-),tersiyse + alıcan.Diğerlerinde mol ilişkisi kurcaksın. 0,2 m ve 400 ml sorularında n.v=m formülü kullanıcaksın.Molarite formülü. 4. soruda Hess Kanunu kullanıcaksın.Burda S gircek G çıkıcağı için ona göre ayarlıyıp birini eksiyle çarpışakcın taraf tarafa toplayınca birbirlerini götürüp elinde S G çıkıcak formül kalcak.Sonra 2 ye bölceksin 1 molu için. Entalpide yani 11.sorunda CHOH işte orda yazıyor CHOH+O2 diycen,H2O + CO2 DİYCEN eşitleyecen.Sonra Ürün-Giren diycen.Örnek:CO2 ORDA ENTALPİSİ (-393) demiş onu işte kaçla denkleştirdiysen onla çarpıcan bu çıkanlar ürün oluyor.CO2+H2O topluyacan sonra CHOH çıkartıcan. Böyle böyle yap.  Nası kimyam iyi dimi Nası kimyam iyi dimi 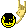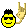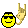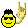 |
Bu mesaja 2 cevap geldi. Cevapları Gizle
| 9-10-11 i çözebildim. kimyada entropiye bile geçemedik okulda. ben konunun başlarından bir test zannetmiştim. Konunun tamamından karışık sormuşlar. hangi kaynak acaba? güzelmiş alıcam da. çözümleri yazayım istersen |
Bu mesaja 1 cevap geldi. Cevapları Gizle
palme kimya 11. sınıf soru bankası , çözümleri yazarsanız sevinirim |
< Bu mesaj bu kişi tarafından değiştirildi Lockheed Martin -- 18 Ekim 2012; 21:22:33 >
Bu mesaja 1 cevap geldi. Cevapları Gizle
hocam soru üzerinde anlatım yapabilir misin böyle pek açıklayıcı olmadı |
|
kesin alıyorum bundan. diğer soruları da bunun kadar güzeldir umarım. öyle mi ? Fiyat neydi aldığınızda? Neyse çözümlere geçeyim. 9. tepkimenin entalpisi 180 kj dür yani 180 kj ısı kullanılmış. 22.5 kj ısı kullanırsak kaç mol no2 oluşur ve kaç litreye denk gelir diyor. 22,5/180= 1/8 eder. tepkimedeki no2 nin katsayısı 2 dir o yüzden 2.1/8=1/4=0,25 mol ediyor. 1 mol 22.4 litre olduğundan 4 te biri 5.6 litreye denk geliyor. 10. tepkimede 1mol=12 gram karbon yanmış ve 394 kj ısı açığa çıkmış. 1.2 gram karbon=0.1 mol karbon yanarsa açığa çıkan enerjiyle 3.94 kg suyu kaç derece ısıtır deniyor. 1 mol karbondan 394 kj ısı açığa çıkmışsa 0.1 molden 39,4 kj ısı açığa çıkar. bundan sonra Q=m.c.deltaT formulünden gidiyoruz. Q joule cinsinden, m gram cinsinden yazılacak. 39.4 kj 39400 joule eder. 3.94 kg 3940 gram eder. 39400=3940.4.deltaT formülü çözünce t 2.5 derece çıkar. 11.ch3oh yanacak ve molar yanma ısısını bulucaz. denklemi yazıp denkleştiricez. ch3oh + 2 o2 ----> co2 + 2 h2o . buna göre oluşum entalpilerini yazıp ürünlerden girenleri çıakrıcaz. -393+ (2(-241)) - (-238) =? işlemin sonucu -637 kj yapıyor. ch3oh 'ın yanma ısısı -637 kj dür anlatabildim mi ? |
Bu mesaja 1 cevap geldi. Cevapları Gizle
sağolun hocam  , kitabın etiketinde 24,5 tl yazıyor kırtasiyeci %20 gibi bir indirim yapmıştı , kitabın etiketinde 24,5 tl yazıyor kırtasiyeci %20 gibi bir indirim yapmıştı |
Bu mesaja 1 cevap geldi. Cevapları Gizle
estağfrullah hocam. fiyatı ıyıymış bari ben 17-18 liraya bulurum onu, haftasonu alıcam:D . Kolay gelsin |
Bu mesaja 1 cevap geldi. Cevapları Gizle
| Yarın muhtemelen alırım kitabı hepsini çözüp atarım aksilik olmazsa. |
Bu mesaja 2 cevap geldi. Cevapları Gizle
|
2. soruda sisteme iş yapılmış(+350) -- Sistem iş yapsaydı -350-- Sistem dışarı ısı vermiş (-200), ---sisteme ısı verilseydi+200-- = 150 |
Bu mesaja 1 cevap geldi. Cevapları Gizle
|
@natrium bekliyorum hocam @Schlaf Schön teşekkürler |

< Resime gitmek için tıklayın >
< Resime gitmek için tıklayın >
DH forumlarında vakit geçirmekten keyif alıyor gibisin ancak giriş yapmadığını görüyoruz.

Üye Ol Şimdi DeğilÜye olduğunda özel mesaj gönderebilir, beğendiğin konuları favorilerine ekleyip takibe alabilir ve daha önce gezdiğin konulara hızlıca erişebilirsin.